外泌體和其他小細胞外囊泡 (sEV) 是細胞間通訊和代謝調節的重要介質,包含蛋白質、編碼和非編碼 RNA、DNA和代謝物,存在于生物體的體液中,包括血漿/血清、尿液和腦脊液。sEV內容物受生理和病理狀態影響,因此它們可用作診斷和預測多種疾病預后的標志物。過去的研究主要針對sEV中miRNA,而對蛋白質組的研究較少。本文作者利用質譜技術研究不同細胞系分泌sEV中的蛋白質組特征,發現不同細胞類型的sEV中蛋白質的獨特性質,以及這些蛋白質的表達水平如何用作識別組織來源的生物標志物。
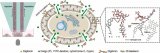
02圖解摘要
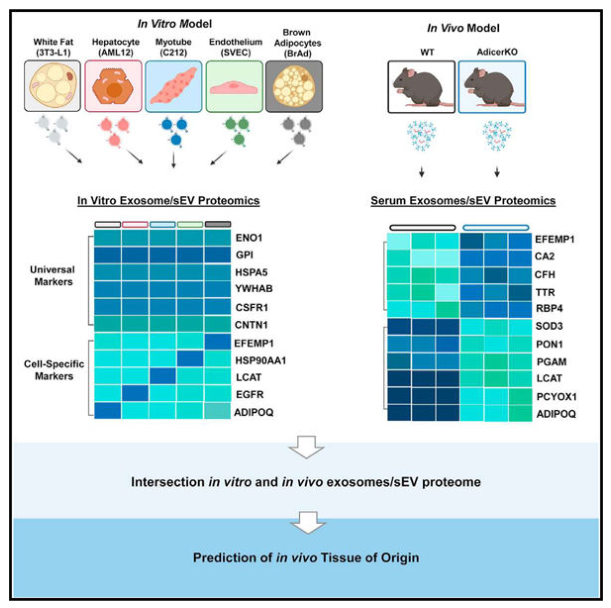
通過比較蛋白質組學,作者確定了來自多種細胞類型的外泌體/sEV共有的標志物,以及每種細胞類型獨有的標志物。使用脂肪營養不良小鼠模型,揭示了sEV蛋白質組數據集來預測體內循環外泌體/sEVs的起源組織的用途。
03研究內容
1、細胞產生的sEVs具有不同的蛋白質組特征
研究者從5個代謝調節小鼠模型細胞系提取外泌體和sEVs,大小在50到200納米之間,并通過NTA分析確定大小分布在5個細胞系中沒有區別,但各細胞系釋放顆粒的速度有很大區別,分化的3T3-L1釋放sEVs最快,而分化的C2C12釋放的最慢。為了探究這些不同細胞釋放的sEVs中蛋白質組的差異,研究者利用LC-MS/MS質譜技術分析蛋白質組成,共鑒定到431種蛋白質。GO富集分析結果表明這些蛋白質多為胞外蛋白(細胞表面或分泌蛋白),或位于細胞質和質膜上,功能上主要參與蛋白質代謝、大分子處理、信號轉導和應激反應。利用PCA分析將5個細胞系分為2個clusters,一個包含C2C12(肌管)和AML12(肝細胞),一個包含3T3-L1(脂肪細胞)、BrAd和SVEC(內皮細胞)。通路富集分析表明,內皮細胞與白色和棕色脂肪細胞釋放的sEV富集了參與分解代謝過程和有機酸、羧酸、氮化合物代謝的蛋白質,且差速離心法分離出的sEVs中檢測到了10種糖酵解途徑中的酶。內皮細胞與棕色和白色脂肪細胞的sEVs富集了脂肪酸合成和脂蛋白代謝的重要酶蛋白。肝細胞和肌管釋放的sEVs參與細胞遷移/黏附、免疫反應、細胞結構調節和脂質與甘油磷脂代謝。這些結果表明,盡管這些細胞系存在顯著的代謝差異,但它們的sEVs中蛋白質組存在意想不到的相似性,將這些細胞系分成2種模式。
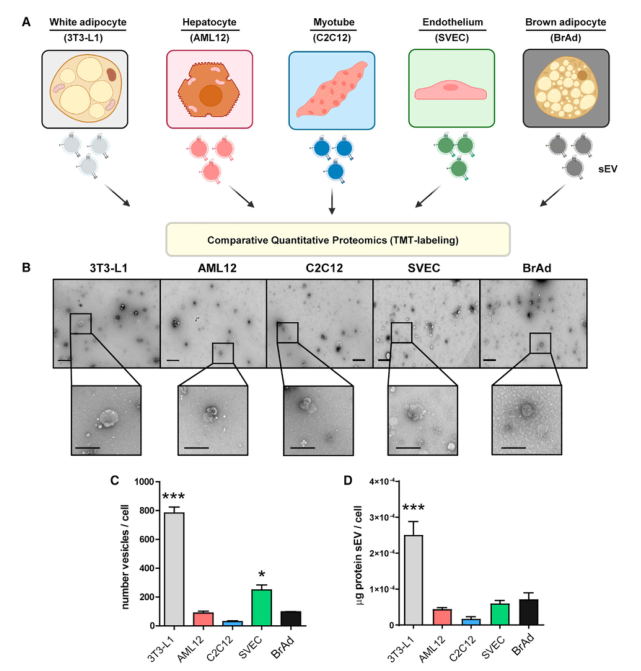
Fig.1 實驗設計和各細胞類型釋放的sEV的表征
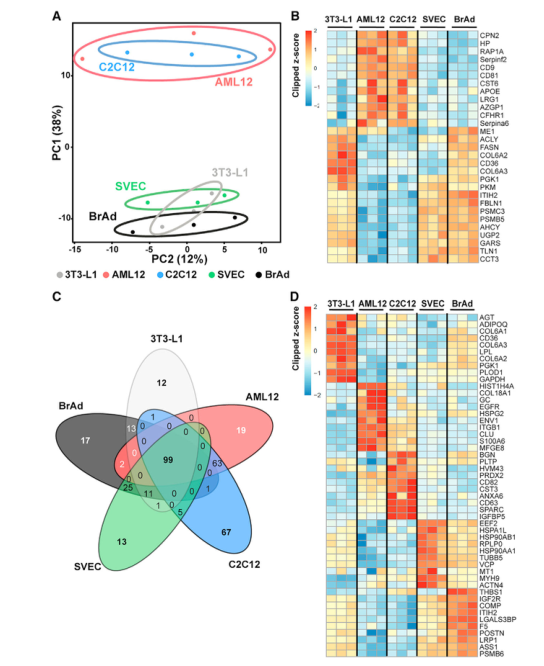
Fig.2 在分離的sEV中觀察到的蛋白質組表達模式
2、不同細胞系sEV蛋白marker鑒定
Tetraspanins家族蛋白CD63、CD9和CD81,在過去研究表明,在sEV中表達豐富,因此常常被用作sEV鑒定、定量或純化的marker。然而,在研究者的結果中,這三個蛋白質在不同細胞系中的表達水平有很大差異。脂肪和肌管細胞系中的sEVs表達水平高,但在內皮細胞和白色與灰色脂肪細胞中表達水平低。相反,研究者從自己的質譜結果中鑒定到6個在sEV中表達水平相似的蛋白質,可能是更好的sEV蛋白marker,分別是ENO1、GPI、HSPA5、YWHAB、CNTN1和CSF1R。前四個蛋白質被預測定位于sEV管腔,后兩個被歸為膜蛋白,因此也可以作為表面marker。
用WB對5種細胞系特異性表達的蛋白質進行分析,鑒定了每個細胞類型的特異性marker,即3T3L1:ADIPOQ、CD36;AML12:EGFR、ITGB1;C2C12:SPARC、IGFBP5;SVEC:HSP90;BrAd:POSTN、THBS1。此外,進入sEVs的蛋白質可能與這些蛋白質在細胞類型的豐度和外泌體分泌通路有關。WB結果表明,一些蛋白質在sEV和細胞的表達水平成比例,如ADIPOQ、SPARC、FASN、IGFBP5。而其他一些蛋白在某些細胞類型的sEVs中與其他細胞類型相比顯著上調,而在細胞表達水平相似,表明存在細胞類型特異性機制使得這種蛋白被分選進入sEV中。從培養細胞和原代細胞提取sEV并用質譜分析蛋白質組,發現培養細胞(3T3-L1)sEV特異表達的蛋白也富集在原代細胞sEV中,表明兩種來源的sEV蛋白質組非常相似。
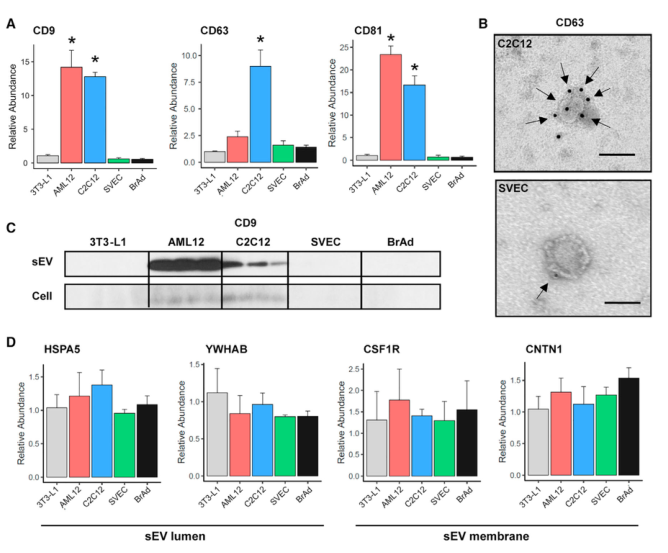
Fig.3 Tetraspanins在不同細胞類型的sEV中表達并不相同
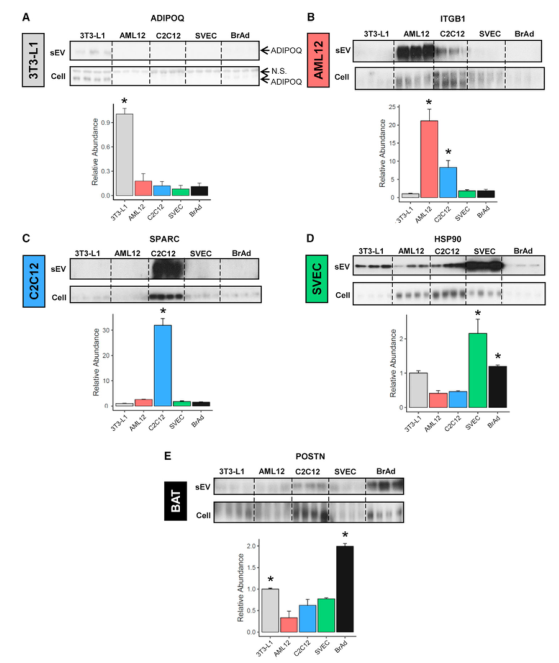
Fig.4每種細胞類型SEV標志物的免疫印跡
3、血清sEV蛋白作為代謝性疾病組織變化的指標
為了確定sEV蛋白質組是否發生改變并可能有助于代謝表型,研究者從12周大的對照和 AdicerKO小鼠中分離出血清sEV,并對它們進行比較蛋白質組學分析。其中86個蛋白質在對照和KO小鼠之間表達不同,AdcerKO的sEV中40個上調和46個下調。富集分析表明上調通路top10中包含視黃醇代謝和補體激活途徑,下調通路top10中包含炎癥反應和鐵代謝。有趣的是,表達水平高度變化的蛋白質包括通常由肝臟、脂肪和其他組織分泌的蛋白質。為了追蹤AdicerKO sEV中顯著改變的蛋白質的來源,研究者將這些蛋白質中的每一種與前文確定的細胞類型特異sEV蛋白質的體外數據交互分析,發現其中三種在KO模型中上調的蛋白來自肝細胞,只有一種蛋白質來自SVEC且在KO模型中上調表達,25種蛋白質來自肌肉細胞,其中12種上調,13種下調。重要的是,有5種蛋白可能是脂肪細胞特異的,且這些蛋白在sEV的表達變化與對應組織中該蛋白的表達水平變化一致。這些數據表明,血清sEV中蛋白質豐度的變化可以反映組織質量和組織中蛋白質表達的變化,這些組織選擇性地將這些蛋白質輸出到它們的sEV中。
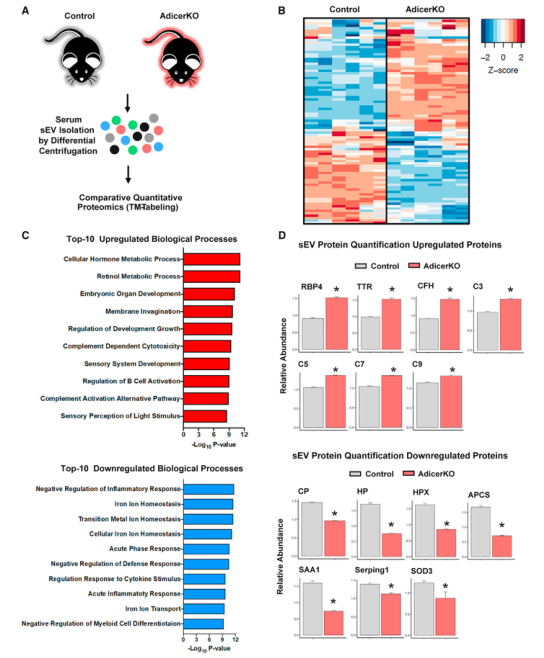
Fig.5 AdicerKO小鼠血清sEV蛋白質組的變化
4、脂聯素作為白色脂肪細胞sEV的標志物
脂肪因子ADIPOQ是一種重要的胰島素增敏劑,由脂肪細胞獨特分泌,是白色脂肪sEV獨特的標志物。HMW脂聯素是其主要的生物活性形式,在與其受體AdipoR1/2結合時,以組織依賴性方式激活AMPK或PPARγ通路。此外,HMW脂聯素與內皮細胞中的 T-鈣粘蛋白結合,調節血管形成,并已被證明可刺激sEV釋放。免疫金標法證實sEV中存在ADIPOQ,sEV分離前后血清進行WB和ELISA分析發現血清中的大部分ADIPOQ是游離的,sEV組分中僅存在一小部分,其主要存在形式為MMW和HMW。在AdcerKO小鼠中,血清和sEV中兩種形式的豐度均有所下降。考慮到對照和AdicerKO小鼠的sWAT中的ADIPOQ蛋白表達相似,這可能是由于在KO組中觀察到的脂肪營養不良而發生的。為了確定sEV中的ADIPOQ是在囊泡表面還是在囊泡內腔中,研究者在用Triton X-100破壞囊泡膜之前和之后都用蛋白酶K處理了sEVs,發現蛋白酶K能夠在添加去污劑前后消化與sEV相關的ADIPOQ。因此,ADIPOQ是位于這些sEV外膜上的白色脂肪細胞sEV的獨特標志物,有可能與 ADIPOQ受體結合并影響這些外泌體/sEVs的靶向性。
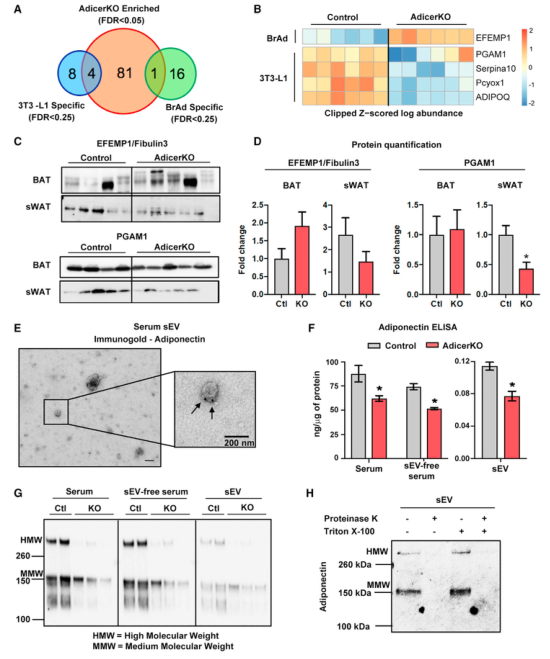
Fig.6 高分子量ADIPOQ在AdicerKO小鼠sEV中表達下調
04結果總結
本研究對可代表重要代謝組織的五種細胞系進行定量蛋白質組分析,發現每一種細胞類型都有獨特的sEV蛋白質組表達模式。雖然 CD9/CD63/CD81等經典sEV標志物的豐度差異很大,但研究者還確定了六種sEV標志物(ENO1、GPI、HSPA5、YWHAB、CSF1R 和CNTN1)。它們在所有細胞類型的sEV中豐度相似。此外,每種細胞類型都有特定的sEV標志物。使用白色脂肪組織減少和棕色脂肪組織增加的脂肪特異性Dicer敲除小鼠,研究者證實這些細胞類型特異性標志物可以預測血清sEV的變化起源。這些結果為了解在代謝穩態中重要的細胞和組織的sEV蛋白質組、識別獨特的sEV標志物以及證明這些標志物如何幫助預測血清sEV的組織來源提供了寶貴的資源。
審核編輯:郭婷
-
編碼
+關注
關注
6文章
957瀏覽量
54953 -
DNA
+關注
關注
0文章
243瀏覽量
31136
原文標題:學術動態 | NTA +LC-MS/MS組合在外泌體蛋白質組研究的應用
文章出處:【微信號:SBCNECB,微信公眾號:上海生物芯片】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
淺談瑞盟科技·MS2583/MS2583M——低功耗、5Mbps、RS-422 接口電路

淺談瑞盟科技·MS2581/MS2581M——低功耗 RS-422 接口電路

MS8241/MS8242——高速、高輸出電流、電壓反饋放大器

MS5182N/MS5189N——16bit、4/8 通道、250kSPS、 SAR 型 ADC

MS5198T/MS5199T——低噪聲、低功耗、16/24 位 ∑-Δ ADC

MS5196T/MS5197T——低噪聲、低功耗、16/24 位∑-ΔADC

差示掃描量熱儀測試蛋白質的應用案例

創客中國AIGC專題賽冠軍天鶩科技:AI蛋白質設計引領者

MS3142/MS3142S 馬達驅動 IC 在自動打蛋機研發中的神奇表現

EvolutionaryScale推出基于NVIDIA GPU模型的新型蛋白質研究方案
洪亮團隊在生信期刊JCIM發布最新成果,蛋白質工程邁入通用人工智能時代
天府錦城實驗室在生物傳感與蛋白質測序領域取得重要進展





 NTA +LC-MS/MS組合在外泌體蛋白質組研究的應用
NTA +LC-MS/MS組合在外泌體蛋白質組研究的應用











評論