【研究背景】
目前的電池電解質是可燃的,構成了一個重大的安全挑戰。無溶劑聚合物電解質的開發就是為了解決這個問題,然而它們沒有足夠的離子傳導性,無法在室溫下進行電池操作。雖然凝膠電解質解決了離子導電性的限制,但其中的溶劑分子沒有被錨定,安全功能因此受到影響。
【工作介紹】
本工作將溶劑分子與鹽和聚合物錨定在一起,可以增加電解質的離子傳導性,而不破壞其非可燃性。具體來說,開發了一種液態聚合物電解質,由LiFSI鹽、二甲氧基乙烷(DME)溶劑和用離子溶解分子錨定的聚硅氧烷組成。DME與鹽和聚合物配位,而與鹽一起,它們協同塑化聚合物以增加離子傳導性。
由此產生的不易燃聚合物電解質具有1.6 mS/cm的室溫離子電導率和25°C-100°C的寬操作窗口。受益于其液體性質,該電解質可以與市面上的電極配對,而無需進一步的電池工程。本工作擴展了聚合物電解質的離子傳導范圍,并為下一代安全和可制造的電解質顯示了一個有希望的設計途徑。
【具體內容】
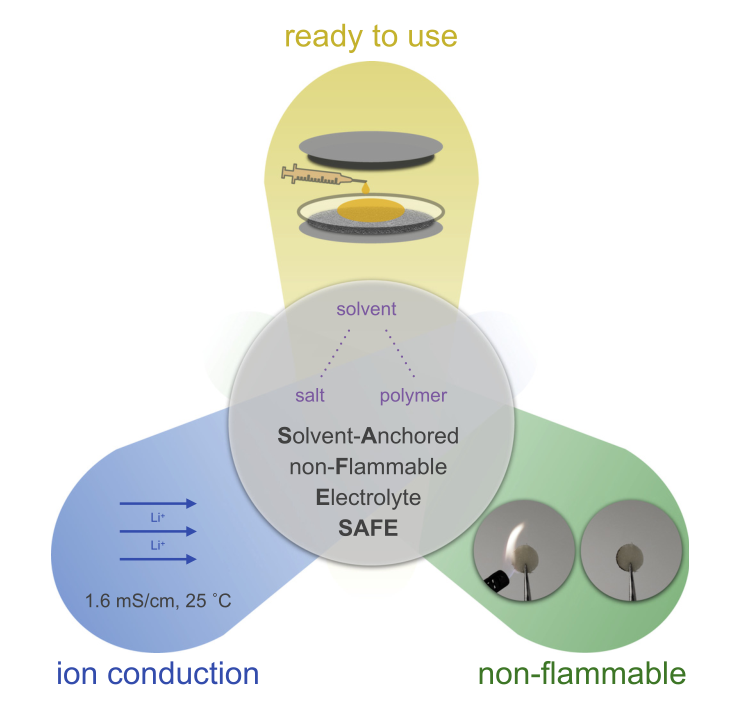
本工作提出了一種基于硅氧烷的聚合物,使用基于離子液體的溶解單元作為聚合物側鏈(溶劑錨定不易燃電解質[SAFE])。靈活的低Tg主干促進了聚合物鏈的運動,提高了離子導電性。通過將離子溶解單元從聚合物骨架移到側鏈上,減少了它們的空間阻礙,使鹽的溶解度更高,從而進一步提高了離子傳導性并降低了這種電解質的粘度。溶劑分子被納入電解質中,以保持高的離子傳導性而不影響其不燃性。這些溶劑存在于與鹽和聚合物高度配位的環境中,不會削弱電解質的安全特性。
由此產生的高鋰鹽含量(鹽:單體=8:1)的電解質,在配位的DME(二甲氧基乙烷)分子的存在下,是一種液體,在25℃時的離子電導率為1.6 mS/cm。與固態電解質(陶瓷或聚合物)相比,SAFE很容易與電極形成親密接觸,并且可以與市售的鎳-錳-鈷(NMC)氧化物陰極配對,無需進一步的電池工程。
通過將離子液體單元拴在聚合物側鏈上,而不是使用小分子離子液體,限制了系統中非鋰陽離子的移動,實現了高的鋰遷移數(~0.7)。證明了SAFE與NMC陰極和石墨陽極在25°C(C/10和C/3)下的穩定循環,超過400次,容量衰減可以忽略不計。這種電解質可以在廣泛的溫度范圍內以實際的電流密度運行(25℃,0.27 mA/cm2 ,100℃,5.4 mA/cm2 ),并為聚合物電解質設定了導電性和性能標準。
材料設計
設計了一種由非極性硅氧烷骨架和吡咯烷(Py)雙(氟磺酰)亞胺(FSI)極性離子側鏈組成的兩親性聚合物電解質,如圖所示 圖1A,將該聚合物命名為PPyMS-FSI。選擇硅氧烷骨架是因為它的化學穩定性和鏈的靈活性。選擇PyFSI離子組是因為它的氧化穩定性和溶解鹽的能力。
其他基于離子液體的聚合物電解質也得到了研究,特別是以聚合PyFSI離子液體作為聚合物骨架,以LiFSI(PDADFSI-LiFSI)作為鹽。本工作聚合物電解質PPyMSMS-LiFSI在25℃時的離子電導率為8.3 × 10?2 mS/cm,較高的電導率源于硅氧烷聚合物骨架的低剛性。在這項研究中,通過將離子溶解基團移到聚合物側鏈上,減少了離子液體的空間阻礙,增加了PyFSI單元與鹽和溶劑配位的自由度(圖1B)。
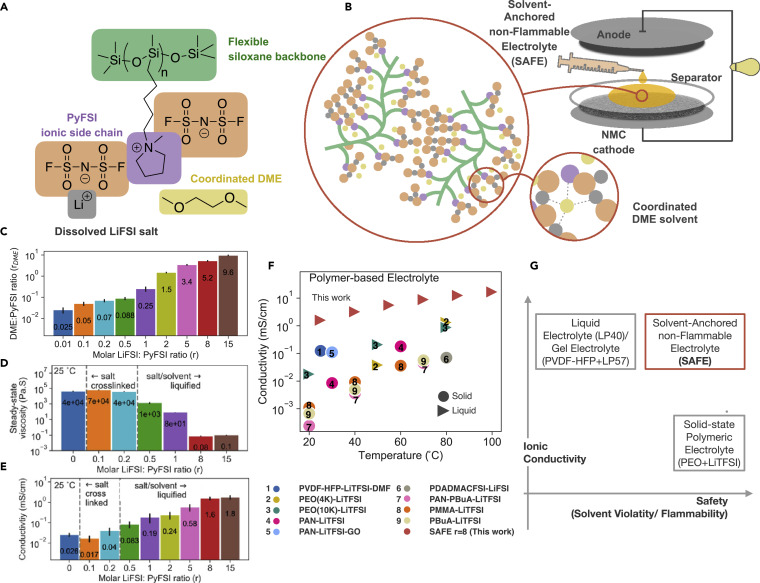
圖1.不同鹽/溶劑比例的SAFE。
(A)以LiFSI:PyFSI:DME=1:1:1的摩爾比繪制的電解質化學結構示意圖。(B)SAFE添加到電池隔膜中,以及復合物的放大漫畫(以LiFSI:PyFSI:DME=2:1:1.5的摩爾比繪制)結構。(C)隨著鹽含量的增加,干燥48小時后電解質中的DME含量。數據以平均值±SD表示。(D) 電解質的離子電導率隨著鹽含量的增加而增加,在25℃下測量。數據以平均值±SD表示。(E) 電解質的穩態粘度。數據以平均值±SD表示。(F) SAFE r = 8在不同溫度下的電導率,并與其他干式鹽中聚合物電解質進行比較。(G) 展示SAFE獨特優勢的示意圖。
電解質成分的優化
SAFE是通過將LiFSI鹽溶解在DME中和將PPyMS-FSI聚合物溶解在ACN(乙腈)中制備的。在真空爐中干燥48小時后,ACN可以完全去除,DME與聚合物和鹽形成配位結構。用1H核磁共振(NMR)對不同鹽濃度的電解質進行了定量分析,并在圖1C中標記為rDME (DME和側鏈的摩爾比)。鹽含量r,它被定義為所添加的LiFSI鹽和PyFSI聚合物側鏈之間的摩爾比。
對于SAFE r = 8電解質,通過將干燥時間從48小時增加到96小時和144小時來優化系統中的DME量。從48小時到96小時,DME量(rDME )從5.25下降到2.53,但粘度從0.08 Pa.S增加到0.20 Pa.S,電導率從1.6 mS/cm下降到0.54 mS/cm。進一步延長干燥時間(144小時)導致鹽分沉淀,而沒有完全去除DME。在干燥時間為48小時時,體系中的DME是降低粘度和促進離子傳導的最佳選擇。
液態聚合物電解質
SAFE的機械性能和離子電導率不僅受溶劑的影響,也受鹽含量的影響。在25°C時,測量了不同r值的聚合物復合物的穩態粘度(圖1D)和離子傳導性(圖1E)。由于PyFSI側鏈的離子性質,對純PPyMS-FSI聚合物(一種粘稠的液體)的EIS(電化學阻抗光譜)測量顯示,在25℃時,離子電導率為2.6 × 10?2 mS/cm。
當少量的LiFSI鹽被添加到聚合物基體中時(即r=0.1-0.2),Li+與聚合物上的離子側基建立了多配位結構,從而使聚合物鏈靜電交聯,限制了聚合物鏈的運動。在r = 0、r = 0.2和r = 0.5的復合物上用隨頻率變化的流變學來表征這種鹽交聯行為。無鹽的聚合物(r = 0)在整個頻率范圍內顯示出液體般的流變特性,損失模量(G″,液體特性)高于儲存模量(G′,固體特性),而r = 0.2在8.5 rad/s時有一個G′和G″的交叉,顯示出粘彈性固體般的行為。進一步增加鹽和溶劑含量(r≥0.5)導致電解質在整個頻率范圍內再次變成液體,G″高于G′。固/液轉換也反映在粘度和離子傳導率的變化上:聚合物/鹽混合物的穩態粘度從4×104 Pa?S(r = 0)增加到7×104 Pa?S(r = 0.1),然后下降到8×10?2 Pa?S(r = 8);電導率從2.6×10?2 mS/cm(r = 0)下降到1.7×10?2 mS/cm(r = 0.1),然后上升到1.6 mS/cm(r = 8)。差示掃描量熱(DSC)曲線中,觀察到PPyMS-FSI聚合物的Tg 在-25℃,而SAFE r = 8樣品的Tg 在-64℃,接近沒有離子相互作用的聚二甲基硅氧烷(PDMS)聚合物的Tg 。這些結果表明,添加的LiFSI鹽和DME可以促進聚合物鏈的運動,限制聚合物側鏈之間的離子相互作用。
將鹽含量從r = 8增加到r = 15對離子傳導性的影響有限。盡管rDME 從5.2增加到9.6,但DME和LiFSI之間的比率仍然相似(r = 8為0.65,r = 15為0.64)。在較低的鹽含量r = 5時,DME和LiFSI之間的比率更高(0.68)。這表明在r = 8時已經達到了該系統的鹽溶解極限。進一步增加鹽含量需要加入相應比例的DME溶劑。
EIS結果通過使用Arrhenius方程擬合r = 8的電導率和溫度信息,計算出離子傳輸所需的活化能為264 meV。當把SAFE r = 8的電導率與其他鹽中聚合物電解質進行比較時,這種電解質在25℃至100℃的整個溫度范圍內顯示出最高的離子電導率。
具體而言,最近關于基于PVDF-HFP LiTFSI的聚合物鹽基電解質的帶有13wt%的殘留DMF。該電解質仍然是固體,并顯示出0.124 mS/cm的室溫離子傳導率。對于短鏈聚乙二醇(聚氧化乙烯[PEO],分子量為10K),它也可以通過添加LiTFSI鹽(Li:單體=0.125)來液化,并且在20℃時的粘度為55PaS。然而,由于其有限的離子溶解能力,液化的PEO電解質在30°C時只能達到0.06 mS/cm的離子傳導率。
通過調整LiFSI和DME的用量,在不影響電解質安全特性的情況下保留了離子導電性。SAFE同時解決了傳統液體/凝膠電解質的溶劑可燃性問題和固態聚合物電解質的離子導電率限制(圖1 G)。
FSI、Li和DME的化學環境
鋰陽離子和FSI陰離子的化學配位環境隨著電解質成分的變化而變化。拉曼光譜可以測量鍵的特定振動模式的能級偏移,然后可以推斷出該鍵的化學環境的變化。在這個系統中,聚合物的離子側鏈和添加的鋰鹽都含有相同的FSI陰離子。如圖所示 圖2A中所示,在純PDMS-PyFSI聚合物中測得的S-N-S鍵的振動能量為~711 cm?1 ;在結晶LiFSI鹽樣品中,該能量為~762 cm?1 。
這些結果與LiFSI鹽和吡咯烷FSI離子液體的S-N-S鍵拉曼信號相似。隨著鹽和溶劑含量的增加,S-N-S鍵信號轉移到更高的文數,表明FSI陰離子的配位環境更強。拉曼光譜發現與傅里葉變換紅外光譜(FTIR)得到了進一步的證實,觀察到含有S-N-S鍵拉伸振動的區域(圖2B)。隨著鹽含量的增加,FTIR中的鍵波數在Li與FSI結合的方向上有所增加,但在結晶LiFSI的能量上沒有觀察到峰值。
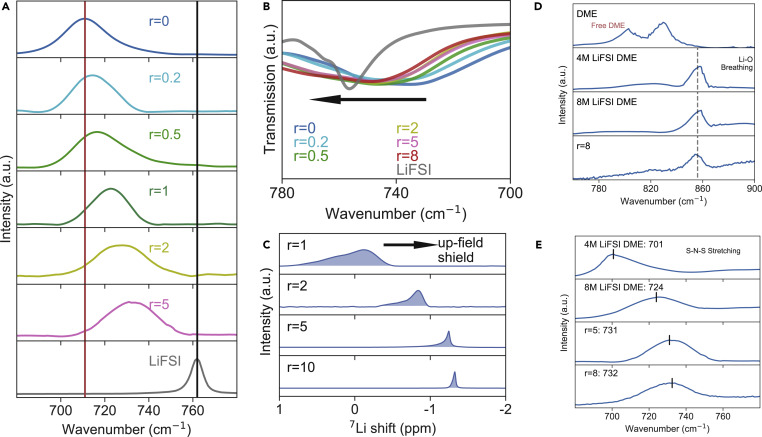
圖2.Li+ , FSI? , DME的配位環境。
(A)聚合物-鹽復合物的拉曼光譜集中在FSI陰離子上的S-N-S鍵的振動模式。(B)聚合物-鹽復合物的傅里葉變換紅外光譜(FTIR)集中在FSI陰離子上S-N-S鍵的振動模式的信號范圍。(C) 在25°C測量的不同鹽含量的聚合物的Li核磁共振(NMR)信號。(D) 拉曼光譜聚焦于DME振動,并標出Li-O呼吸鍵。(E)拉曼光譜聚焦S-N-S鍵拉伸,與4和8M LiFSIDME溶液(進料成分)相比。
應用核磁共振研究了Li陽離子的化學環境。在圖2C中,隨著聚合物中鹽含量的增加,鋰峰呈現出上場轉移。上場轉移表明,由于周圍的電子云密度較高,鋰核的屏蔽性更強。與拉曼和FTIR的觀察一致,系統中鹽含量的增加導致了更配位的溶解環境。隨著鹽含量的增加,核磁共振峰的寬度下降,這是由于電解質的粘度降低造成的。此外,高鹽濃度下Li核的尖銳峰值(r = 8)也表明,添加的Li鹽完全溶解在基體中,并存在于一個均勻的化學環境中。
用拉曼光譜對SAFE中DME的溶解環境進行了表征,并與高濃度LiFSIDME電解質進行了比較。圖2D顯示了DME的振動信號。當DME中沒有LiFSI時,純DME在幾個確認中存在,導致兩個明顯的拉曼峰,其波數低于850 cm?1 。在4和8M LiFSI DME電解質中,Li-O峰出現在856 cm?1 ,表明Li陽離子與DME上的氧進行配位。
在r=5和r=8的電解質中,FSI陰離子的配位環境也與4和8M LiFSI DME電解質進行了比較(圖2 E)。當鹽濃度從4M增加到8M時,峰值位置從701 cm?1轉移到724 cm?1 。與不含聚合物的DME電解質相比,SAFE中的S-N-S拉伸進一步藍移至>730 cm?1 ,表明PPyMS-FSI聚合物也對高配位環境做出了貢獻。
對r=1的電解質(LiFSIDME=10.25)進行了MD模擬,并分析了徑向分布函數(RDF)來研究電解質成分之間的相互作用。在短距離(<1納米),g(r)峰的值大于1,表明感興趣的兩個成分之間的相互作用,因為所選成分在參考成分附近的局部密度大于其在大塊電解質中的濃度。
Li+ 與FSI? 中的氧原子和DME中的氧原子都顯示出強烈的相互作用,在RDF中有明顯的峰值。FSI? 與Li+ 有強烈的相互作用,但與DME沒有明顯的相互作用。除了與Li+ 相互作用外,還發現DME與聚合物側鏈上的Py+ 基團有相互作用。總的來說,MD模擬結果與實驗結果一致,即DME被固定在一個高度配位的富鹽環境中,并且DME與Li+ 和聚合物都有相互作用。任何兩個成分之間的平均力潛力(PMF)可以通過關系w(r)=-kB T ln(g(r))從RDF計算出來。PMF的最小值的大小是對兩個成分之間相互作用強度的定量測量。
可以發現,DME上的氧與其他成分的配位性最強,因此被用來計算DME的相互作用強度。計算了Li+ -O(DME)和N(聚合物)-O(DME)相互作用的PMF,發現Li+ -O(DME)的相互作用強度為0.25 kB T,而N(聚合物)-O(DME)的相互作用強度為0.17 kB T。因此,DME與聚合物的相互作用強度略低于DME與Li+ 。這兩種相互作用都弱于由Li+ -O (FSI? )PMF代表的離子計數相互作用,后者的強度為1.30 kB T。因此,這些相互作用可能不會強烈阻礙DME或Li+ 在溶液中的移動。
穩定性、反應性和電化學特性分析
選擇SAFE r = 8進行進一步的電化學研究。在將其應用于電池的長期循環之前,首先分析了這種電解質在鋰-鋁電池中的氧化穩定性。對電池進行了線性伏安測試,確定SAFE r = 8電解質的氧化電壓為6.7V,與Li (圖3A).這樣高的氧化電位足以與高電壓的NMC電極配對。高氧化穩定性歸功于電解質的高鹽含量和穩定的成分(離子液體)。
接下來,使用擴散有序光譜(DOSY)核磁共振技術,在80°C測量了鋰和氟原子核的遷移數。該電解質的遷移數被計算為0.71,表明該系統中的大部分流動成分是Li+ 。還通過電化學極化測量了Li|Li對稱電池的遷移數,遷移數被計算為0.65。這與DOSY-NMR測量值一致,而且,在這兩次測量中,都假設遵守了Nernst-Einstein關系,系統處于稀釋極限。這是一個簡化的模型,沒有考慮到未分離的離子對/三聯體,但它確實提供了關于電解質中離子運動的有用見解。
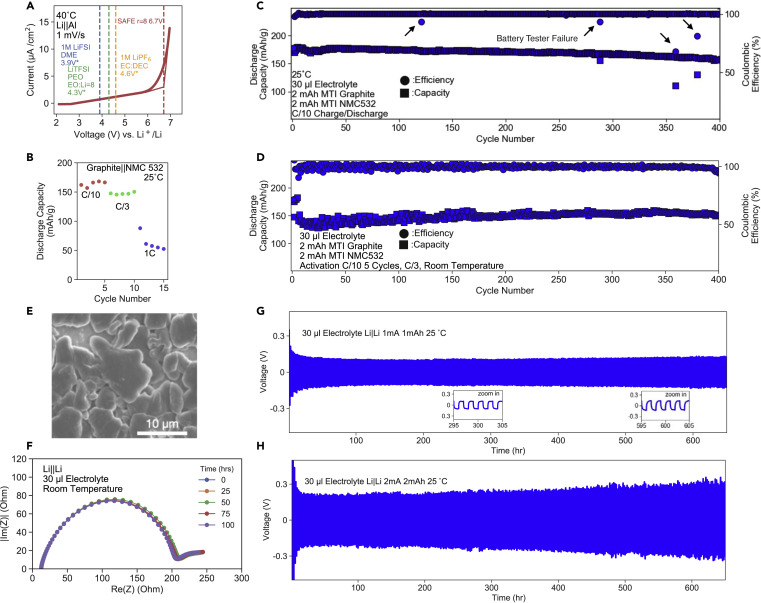
圖3.SAFE的穩定性和電化學特性r=8
(A) 在Li-Al電池中對電解質進行的LSV。測得的氧化穩定性與其他普通聚合物/液體電解質的氧化穩定性進行了比較。(B) 石墨|NMC電池的容量與速率。(C)石墨|NMC電池在C/10速率下的長期循環。(D)石墨|NMC電池在C/3速率下的長期循環。(E)裸銅箔上的鋰沉積形態的SEM圖像(1 mAh/cm2 容量,0.1 mA/cm2 電流密度)。(F) 室溫下各種靜止時間后,SAFE r = 8的Li|Li對稱電池的阻抗測量的奈奎斯特圖。(G) Li|Li電池在1 mA/cm2 電流密度、1 mAh容量下的長期循環。(H) Li|Li電池在2 mA/cm2 電流密度、2 mAh容量下的長期循環。
長期的穩定性和電池應用
接下來研究了該電解質在石墨|NMC全電池設置中的循環情況。這種電解質在C/3時有150 mAh/g的容量,在C/10時有170 mAh/g的容量,當與市面上的NMC陰極(MTI,2 mAh/cm2 )配對時。將這些石墨|NMC電池在貧電解質(30μL)條件下以C/10的速率進行循環,400多個循環的容量衰減可以忽略不計(圖3c)。對于C/3電池,我們也顯示出穩定的長期性能,超過400個周期,沒有明顯的容量衰減(圖3D)。電解質在Li-LNMO電池中循環時也表現出了高電壓穩定性。
評估了電解質與金屬鋰陽極的兼容性。在電流密度為0.1 mAh/cm2 的銅箔上沉積了1 mAh/cm的金屬鋰2 。金屬鋰的掃描電子顯微鏡(SEM)沉積曲線(圖3E)表明,沉積的金屬鋰的形態是顆粒狀的和均勻的。放大的SEM圖像表明,這種形態在電極上的大面積觀察到。
固體-電解質界面(SEI)的穩定性是通過使用EIS測量跟蹤Li|Li對稱電池在很長一段時間(~100小時)內的界面阻抗來進一步描述的。在室溫下靜置100小時后,界面阻抗幾乎沒有變化,這表明金屬鋰和電解質之間形成了一個穩定的界面(圖3F)。
通過在室溫下以不同的電流密度循環Li|Li電池,評估了r=8電解質與金屬鋰的長期穩定性。在電流密度為1 mA/cm2 ,容量為1 mAh/cm2 ,SAFE r = 8電解質顯示出超過700小時的長期穩定循環(圖3G)。在更高的電流密度為2 mA/cm2 ,容量為2 mAh/cm2 ,該電解質表現出超過650小時的穩定循環(圖3 H)。
表征了金屬鋰和石墨陽極在不同的C速率下循環后的SEI的化學成分。在C/10或C/3下循環的石墨陽極具有類似的化學成分,其產品來自鹽(Li2 O, -SOx )和溶劑/聚合物(-O-C)的分解。在1C速率下,充電/放電過程變成了電容性的,并且陽極表面大部分被有機分解產物(-O-C)覆蓋。在金屬鋰陽極上也發現了類似的趨勢,在1C速率下循環的陽極與在C/3或C/10速率下循環的電極相比,其表面化學性質明顯不同。具體來說,在陽極表面出現了更多的聚合物物質,可能是由聚合物或溶劑分解產生的,而由鹽組成的產品較少(Li2O, -SOx )。在50個循環之前和之后,拍攝了石墨|NMC電池的橫截面,在循環之后,SAFE r = 8在電極和分離器上保持濕潤。
熱穩定性和電解質的操作窗口
對電池的長期熱穩定性進行了研究,將電池長期放置在70℃的烘箱中,8天后電導率保持不變。為了證明聚合物對改善電解質的熱穩定性和安全特性的影響,還合成了小分子Py12FSI離子液體,并組成了具有相同摩爾比的DME、LiFSI和PyFSI的小分子基電解質,將其命名為SM。
還比較了聚合物和SM電解質的長期熱穩定性,SM電解質的電導率在70℃熱保持3天后開始下降,而SAFE r = 8的電導率在熱保持8天后保持不變。這些電解質的熱穩定性是通過可燃性試驗進一步評估的。用1 mL SAFE r = 8或碳酸乙烯酯(EC)和碳酸二乙酯(DEC)1M六氟磷酸鋰(LiPF6 )10%碳酸氟乙烯酯(FEC)電解質浸泡。
接下來,我們將火焰噴燈放在浸泡過的玻璃棉附近3秒鐘,然后移開火焰。對于碳酸酯電解質,燃燒一直持續到所有液體被耗盡。對于SAFE r = 8,只在玻璃棉上觀察到輕微的炭化現象(可能是由于鹽和聚合物的降解);更重要的是,燃燒沒有持續。相比之下,SM電解質是可燃的,燃燒一直持續到所有的電解質被燒成黑色物質。
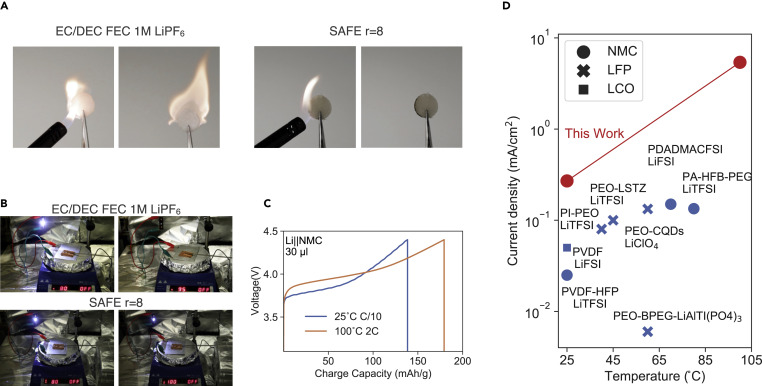
圖4.SAFE的熱穩定性r = 8
(A)用1 mL SAFE r = 8或EC/DEC 1M LiPF6 10% FEC電解質浸泡玻璃棉的快照。火炬與玻璃棉接觸了3秒鐘,然后移開。(B) 帶有SAFE r = 8或EC/DEC 1 M LiPF6 10% FEC電解質的軟包電池在放置在熱板上時操作LED燈的快照,圖片中標明熱板的溫度。(C) 含有30μL SAFE r=8、300μm Li陽極和2.7 mAh NMC 532 Li陰極的Li|NMC電池在25℃下以不同的C速率循環。(D) SAFE r = 8的電流密度與文獻中其他干式聚合物電解質的比較。
對于基于碳酸酯的電解質,當熱板加熱到95°C時,LED突然關閉,這很可能是由于電解質蒸發和降解導致軟包電池中離子傳導通路的損失,使用聚合物基電解質的LED即使在熱板溫度保持在100°C 6分鐘后仍然亮著。
通過記錄發生顯著產氣的溫度,進一步證明了SAFEr=8的熱穩定性。對于EC/DEC電解質,由于DEC分子的揮發性,觀察到軟包電池從105°C開始就被溶劑蒸氣壓脹。聚合物電解質的顯著產氣發生在比鹽分解(140℃)更高的溫度(160℃),表明鹽分解而不是溶劑產氣是電解質熱失效的原因。
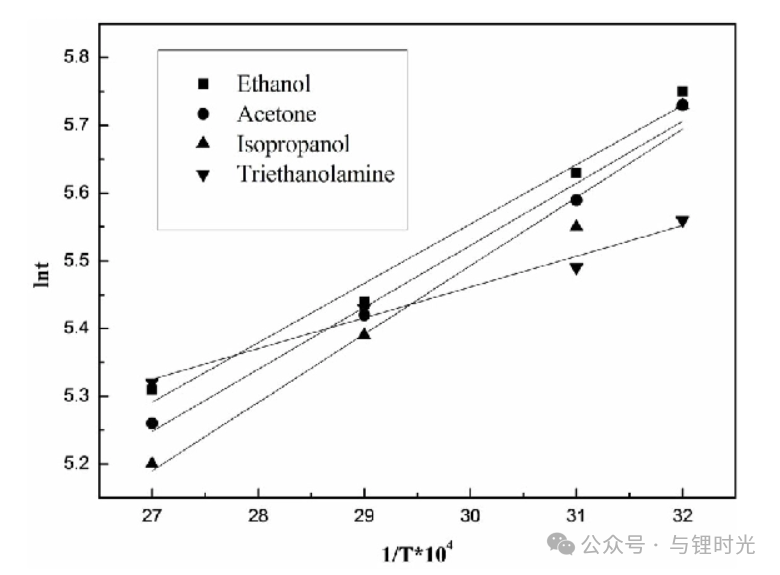
為了量化聚合物電解質系統中DME溶劑的揮發性,并與其他電解質系統進行比較,用氣相色譜室測量了100℃下不同電解質中不同有機溶劑的相對飽和度。通過對氣相色譜儀輸出的溶劑信號峰的曲線下面積進行積分,并計算出電解質和標準溶劑樣品之間的積分比,得到了相對飽和度值。
對于SAFE r = 8的電解質,在真空爐中干燥48小時后,DME的相對飽和度為2%。進一步延長干燥時間到96小時,相對飽和度降低到0.6%。通過測量兩種廣泛報道的基于PVDF-HFP的凝膠電解質中最低沸點成分的相對飽和度,注意到這種聚合物液體電解質與其他經典凝膠電解質之間的差異。
在這兩種情況下,相對飽和度都比我們報道的聚合物電解質要高(38%,80%)。還測量了經典碳酸酯電解質(EC/DEC)和高濃度醚電解質(4M LiFSI DME)的相對飽和度,發現它們的相對飽和度也高了幾個數量級(分別為94%,84%)。還發現SM電解質的DME的相對飽和度是SAFE r = 8電解質的2倍多。這一系列的測量表明,聚合物電解質中殘留的DME的揮發性明顯低于其他凝膠和其他高濃度(基于離子液體)電解質中的有機溶劑。

在25°C和100°C的條件下對NMC鋰電池進行了循環測試(圖4C)。為了達到目標容量130 mAh/g,在25°C,需要 C/10 ,而在100°C,2C就足夠了。這種液態聚合物電解質與市面上的NMC陰極配對在25°C時達到了0.27 mA/cm2 的電流密度,在100°C時達到了5.4 mA/cm2 。
【結論】
作者提出了一個將溶劑分子納入聚合物電解質的概念,以獲得具有高室溫導電性的不易燃聚合物電解質。通過采用硅氧烷主干和離子液體功能側鏈的兩親聚合物設計,提高了聚合物的鹽溶解度。通過調整該電解質中的鹽和配位溶劑的含量,最大限度地提高了離子導電性(1.6 mS/cm,25°C),而沒有破壞電解質的安全功能或熱穩定性。
這種電解質以液態的方式解決了固態電解質(聚合物和陶瓷基)的制造困難,并且可以很容易地與市面上的電極和隔膜整合。該電解質在石墨|NMC全電池中顯示出穩定的長期運行,其運行范圍為25℃至100℃。聚合物電解質的設計理念使下一代安全聚合物電解質的離子傳導性和可制造性得到明顯改善。
審核編輯:劉清
-
電解質
+關注
關注
6文章
820瀏覽量
20158 -
DME
+關注
關注
0文章
22瀏覽量
7433
原文標題:崔屹&鮑哲南Matter:不可燃電解質
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
研究論文::乙烯碳酸酯助力聚合物電解質升級,提升高電壓鋰金屬電池性能

陳軍院士團隊最新Angew,聚合物電解質新突破

一種薄型層狀固態電解質的設計策略




 開發一種不可燃的液態聚合物電解質
開發一種不可燃的液態聚合物電解質











評論